「内なる外」といわれる腸の玄関の仕組み 粘膜面における抗原取り込み機能の分子メカニズムの一端を解明

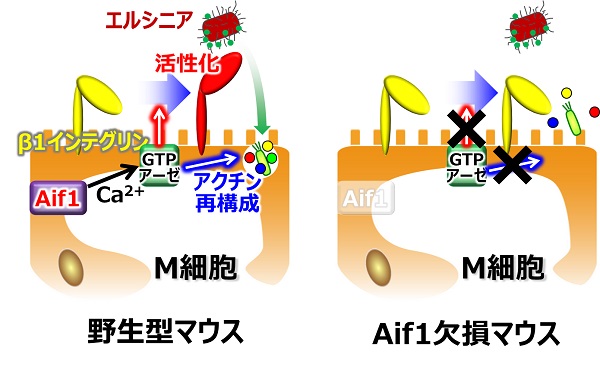
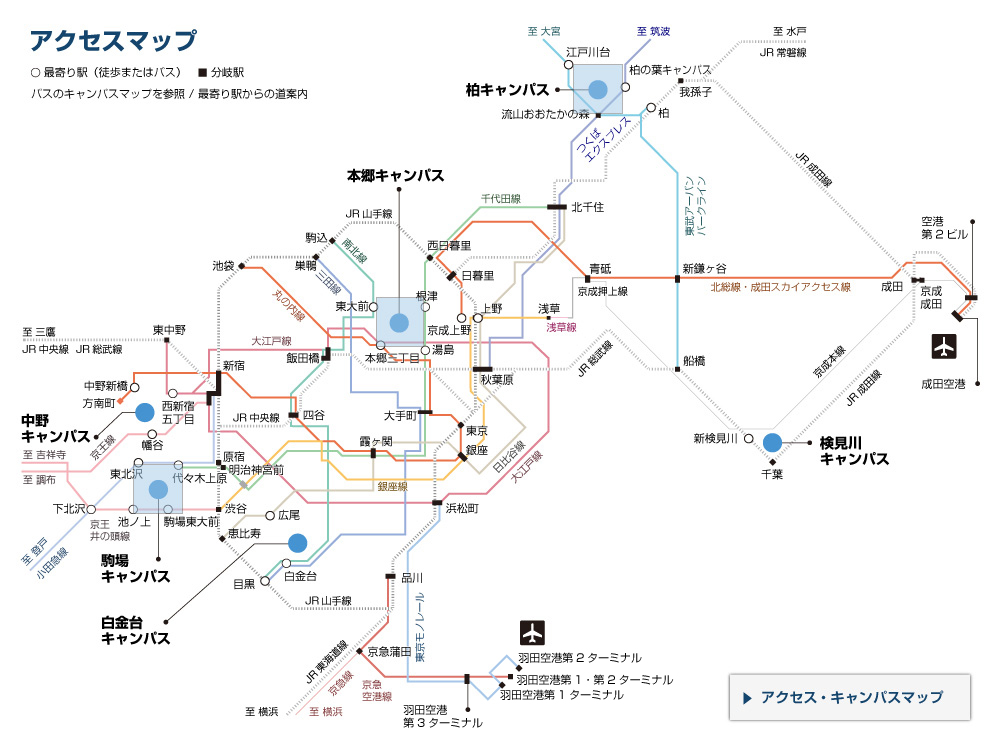
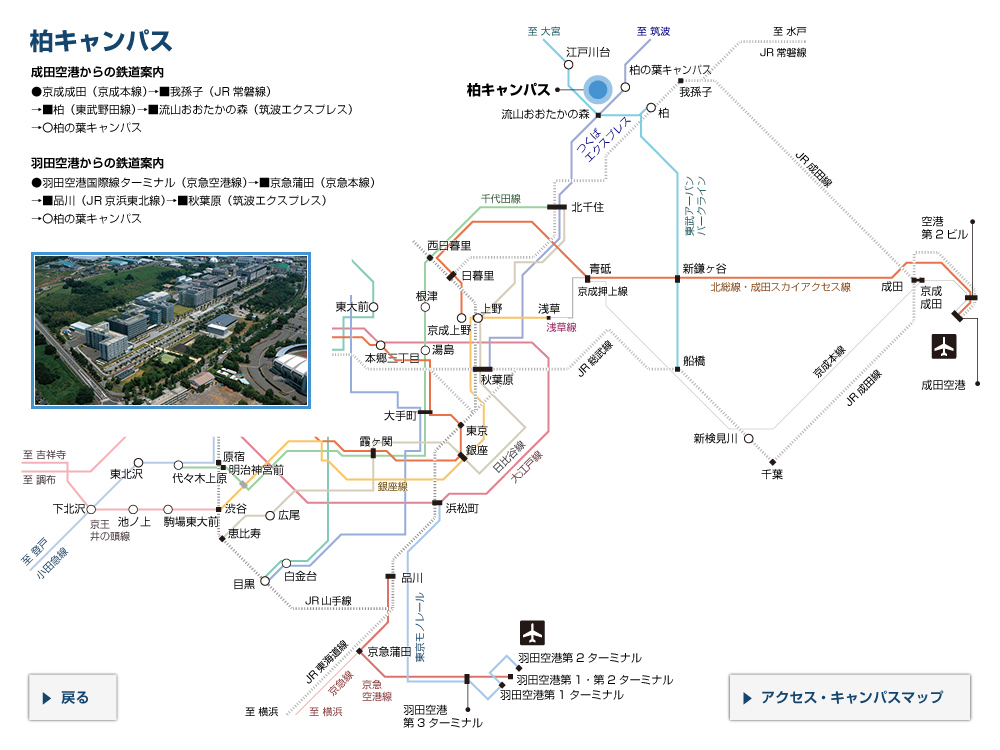
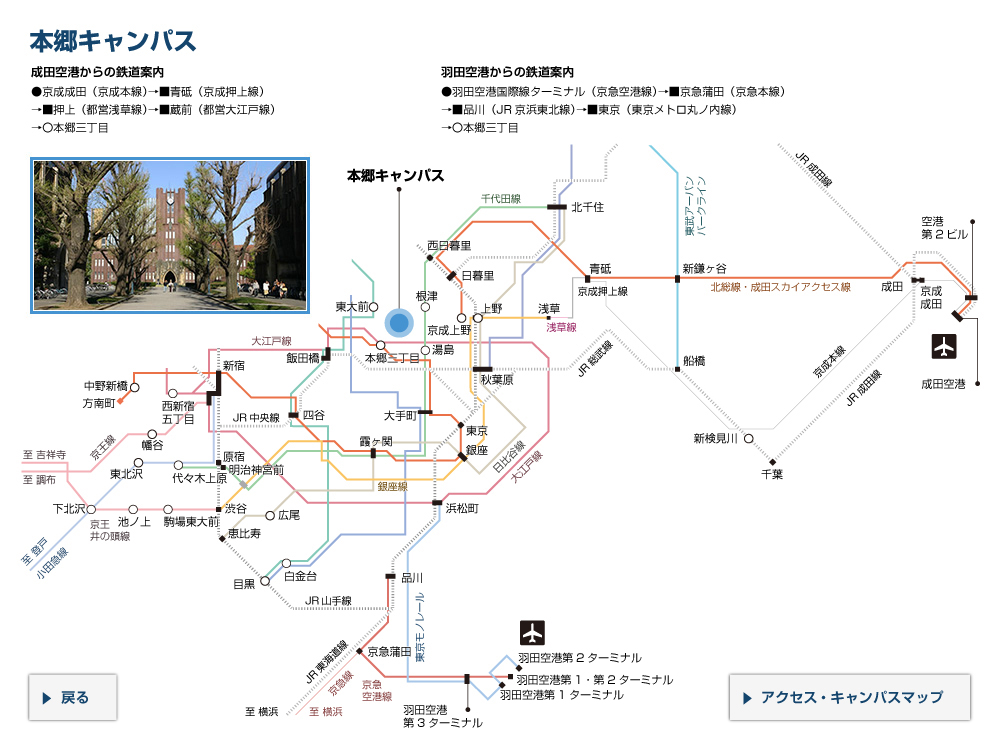
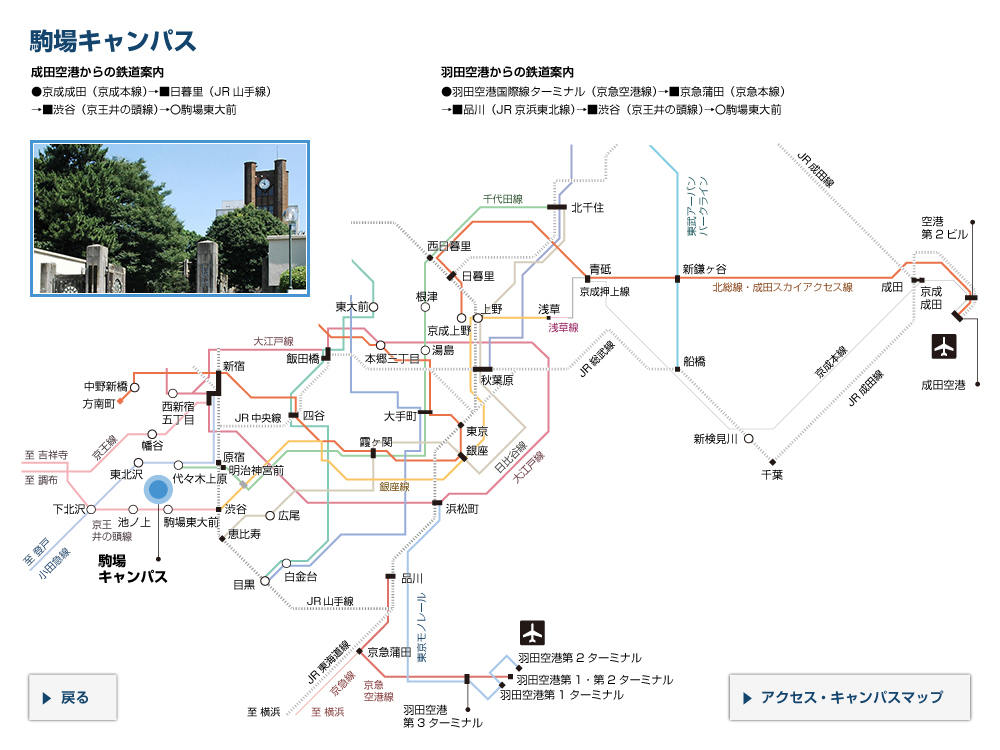
腸内のM細胞におけるAif1の役割
正常なマウス(野生型マウス)のM細胞では、Aif1が発現しており、Aif1はカルシウムイオン依存的にRacに代表される酵素(GTPアーゼ)を活性化する。活性化されたGTPアーゼはアクチン再構成を引き起こし、腸内の内側に向いている細胞膜の形を変化させて抗原を取り込む。またGTPアーゼは、食中毒の原因菌の一種であるエルシニアを認識する受容体(β1インテグリン)を活性化させ、エルシニアの効率的な取り込みを可能にしている。Aif1を欠いたマウスではGTPアーゼが活性化できないために、抗原や病原菌などの取り込み、侵入が起こりにくくなっている。
© 2017 Shintaro Sato.
東京大学医科学研究所の清野宏教授と大阪大学微生物病研究所の佐藤慎太郎特任准教授らの研究グループは、腸の表面などの粘膜面から異物(抗原)を取り込む能力を有するM細胞で、その機能に直接関わるタンパク質としてAif1をマウスにおいて同定しました。本タンパク質を操作できるようになれば、注射型ワクチンに代わって、口や鼻から投与して粘膜に取り込む粘膜型ワクチンに役立つと期待されます。
私たちの身体には、体内に入り込んだ異物を察知して退治する免疫と呼ばれる働きがあります。その一方で、私たちが食べたものを消化する腸などの消化管では、体内に存在するにもかかわらず食べたものや腸内細菌などの異物にさらされています。そこで消化管などの粘膜面では、「良い異物」と「悪い異物」を見分けて応答する粘膜免疫が働いています。腸の表面にある粘膜面では、抗原を取り込みやすくするための落とし穴のような構造があり、その機能を主として担っているのがM細胞と考えられています。これまでに、M細胞には微生物を効率的に取り込むための特殊なタンパク質(受容体)が発現されていることがわかっていました。しかし、M細胞は抗原を一度取り込んで、細胞内を通過させる(トランスサイトーシス)機能を有しているものの、このような機能に直接関与する分子は未だに報告されていませんでした。
研究グループは、M細胞のほとんどを欠いたマウス群と正常なマウス群の腸内の上皮細胞で発現されている遺伝子の解析を行いました。その結果、Aif1タンパク質がM細胞にのみ発現している分子であることがわかりました。そして、Aif1タンパク質を欠損したマウスを作製してAif1タンパク質の機能を調べたところ、Aif1は抗原を取り込む際にM細胞のアクチンの動きを制御することで膜を変化させていることが示唆されました。
「一時的にAif1の機能やその発現をコントロールすることができるようになれば、粘膜型ワクチンの抗原取り込み効率を上げることが可能になります。また逆に、「悪い異物」である病原性微生物の侵入を妨げることができるので、感染予防への応用も期待できます」と清野教授は話します。
プレスリリース [PDF]
論文情報
, "Allograft inflammatory factor 1 is a regulator of transcytosis in M cells", Nature Communications Online Edition: 2017/02/22 (Japan time), doi:10.1038/ncomms14509.
論文へのリンク(掲載誌)