記者会見「癌抑制遺伝子産物である転写因子JDP2によるヒストンアセチル化及びヌクレオソーム形成の制御」の開催研究成果

記者会見「癌抑制遺伝子産物である転写因子JDP2によるヒストンアセチル化及びヌクレオソーム形成の制御」の開催 |
1. 発表日時
平成18年3月3日(金) 午後2時から
2. 発表場所
東京大学 農学部 2号館 1階 115室
3. 発表タイトル
「Regulation of histone acetylation and nucleosome assembly by transcription factor JDP2」
「癌抑制遺伝子産物である転写因子JDP2によるヒストンアセチル化及びヌクレオソーム形成の制御-癌抑制遺伝子産物の新しい活性の発見と癌治療薬開発に新しい視点を示唆-」
4. 発表者
堀越正美(東京大学分子細胞生物学研究所 助教授)
5. 発表概要
i) 基礎科学としての意義
DNA結合性転写調節因子が、従来から考えられているDNA結合活性だけでなく、クロマチン機能制御に重要なヒストンアセチル化の抑制活性及びヌクレオソーム形成活性を有しているといった誰もが予想しなかったことを発見した。
ii) 応用科学としての意義
現在癌治療薬の開発は、裸のDNAレベルでなされてきた成果に基づいたものであったが、本成果は、クロマチンレベルでの新しい研究成果であるため、新しいタイプの癌治療薬の開発が可能となった。
6. 発表内容
我々ヒトを含む真核生物では個々の細胞がヒストンという蛋白質を持ち、DNAはそのヒストンに巻きついて高次に折りたたまれ、クロマチンという立体構造をとっている。遺伝子発現制御に不都合が生じると、蛋白質が正しく作られなくなるため、多くの疾患の原因となっていることが知られており、遺伝子発現制御においてクロマチン構造の制御が非常に重要であることが近年明らかにされてきている。そのため、クロマチンを制御する因子を標的とした新しいタイプの薬剤の開発が期待されている。例えば、アセチル化されたヒストンからアセチル基を除去するヒストン脱アセチル化酵素が働かないようにする薬物が抗腫瘍活性やアポトーシス誘導活性を示すといった興味深い結果が報告されている。このことから、ヒストンアセチル化は癌と密接に関わっていると考えられ、高アセチル化ヒストンを蓄積するヒストン脱アセチル化阻害剤は、新しいタイプの抗癌剤になりうるとの期待が高まっている。これまで基礎研究が遅れていたクロマチンレベルでの新しい知見が得られれば、その成果を元に新しい抗癌剤の開発が進むと考えられている。
特定の塩基配列に結合するDNA結合性転写調節因子JDP2(Jun Dimerization Protein 2)は、癌遺伝子産物c-junやATF-2とヘテロ二量体を形成して標的遺伝子プロモーターに結合し、標的遺伝子からの転写活性を負に制御する。このことから、この蛋白質が癌抑制遺伝子産物として働くと考えられる。このように、生物学的に重要なJDP2の作用機構を探ることは、遺伝子発現制御機構の側面ばかりでなく、細胞機能制御ひいては細胞癌化制御機構の新局面を切り開くことになると期待されていた。今回発表の論文では、JDP2がDNA上のプロモーターのみならずクロマチン構造の主要構成因子ヒストンに結合し、i)ヒストンアセチル化酵素p300による転写活性化に重要な2ヶ所のヒストンのリジン残基のアセチル化を阻害すること、ii)ATF-2と協調して塩基配列特異的にp300によるヌクレオソーム内のヒストンアセチル化反応を阻害すること、そして驚くべきことに、iii)ヌクレオソーム構造形成活性を有することを明らかにした。すなわちDNAに結合し、かつヌクレオソーム構造形成活性を有する因子の発見は、世界で初めてのことである。これらの知見は、ここ10年欧米を中心に最先端研究として鎬が削られてきた染色体からの遺伝子発現制御機構において、新しい研究分野を切り開くことになった。これまで日本から発信するクロマチン研究として唯一世界を先導してきたのがヒストンシャペロン研究分野であり、その中で、JDP2がヒストンシャペロンであると示したことは、和製ヒストンシャペロン因子としてNAP-1、TAF-1、CIA/ASF-1、そしてFKBPの単離・機能解析に次ぐ快挙である。
多機能性因子としてのJDP2の新しい機能の発見は、ヌクレオソーム形成の制御も癌治療薬の標的として重要であることを示しており、癌治療薬開発においてクロマチンレベルでの制御を標的とするといった新しい道を示すものである。
7. 発表雑誌
Nature Structural and Molecular Biology
3月5日にオンラインにて先行掲載。4月号に雑誌掲載。
8. 解禁日時
3月6日午前3時(日本時間)
(米国東部時間3月5日午後1時)
9. 問い合わせ先
東京大学・分子細胞生物学研究所・発生分化構造研究分野
堀越正美
10.用語解説
i) 転写因子
DNA上の特定の塩基配列に結合して転写を制御する蛋白質。
ii) ヘテロ二量体
異なる因子(蛋白質)同士が結合した複合体。
iii) プロモーター
転写酵素RNAポリメラーゼが結合して転写を開始するDNA上の特定の領域。
iv) リプレッサー
特定の遺伝子の発現を抑える働きをもつ制御蛋白質。
v) 細胞周期
細胞分裂とDNA複製に見られる周期。細胞はG1期(DNA合成準備期)、S期(DNA
合成期)、G2期(分裂準備期)、M期(分裂期)を1サイクルとして分裂を行う。
vi) 癌遺伝子産物
遺伝子が変異することによって癌化に関与するようになる因子(蛋白質)。正常対立遺伝子が存在していても細胞の癌化に関与しうる。正常細胞では、癌遺伝子、癌抑制遺伝子はすべて細胞周期や細胞増殖の制御などに関与している重要な機能をもつ。
vii) 癌抑制遺伝子産物
遺伝子が変異することによって癌化に関与するようになる因子(蛋白質)。正常対立遺伝子の欠除があってはじめて,その変異が細胞の癌化に関与しうる。
viii) クロマチン
塩基性の蛋白質であるヒストンにDNAが巻きついたヌクレオソーム構造を基本構成単位とする集合体。クロマチンの状態ではDNAは高次に折たたまれているため、転写抑制状態に置かれる。この状態の形成・解除の制御が転写制御に重要となっている。
ix) ヒストン
DNAと結合してヌクレオソームを形成し、クロマチンの主成分となっている塩基性核蛋白質。
x) ヒストンアセチル化酵素
ヒストンのアミノ酸残基に対するアセチル化修飾を触媒する酵素。
xi) アセチル化
アセチル基がアミノ酸残基に転移されること。ヒストンにおいてはリジン残基がアセチル化される。このアセチル化を目印として、遺伝子発現制御を始めとした様々な染色体における活性が制御されていることが明らかにされてきている。
xii) ヌクレオソーム
クロマチンの基本構成単位である、DNAがヒストンに巻きついた構造。
xiii) ヒストンシャペロン
ヌクレオソームの形成・解除を触媒する酵素。
xiv) c-jun
ニワトリ肉腫ウィルスの持つ癌遺伝子v-Jun類似の遺伝子として分離された癌遺伝子から作られる蛋白質。さまざまな増殖因子やストレス刺激によって転写が誘導される転写因子で、細胞周期やアポトーシスと深い関連があるとされている。
11. 添付資料
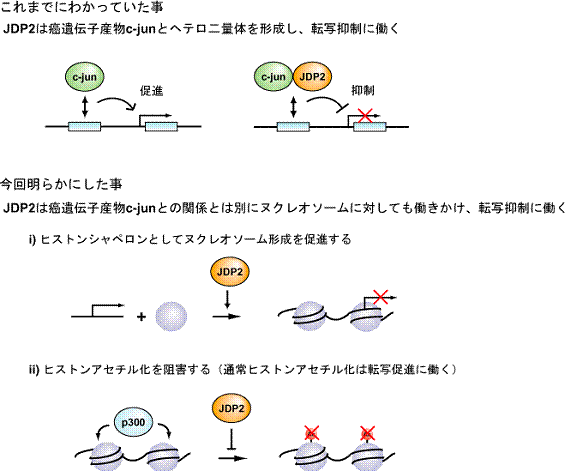
*癌抑制遺伝子産物であるJDP2は、DNA結合性因子として示すリプレッサー型の転写抑制反応だけでなく、ヌクレオソーム構造を介した転写反応をも阻害する活性を有していることを明らかにすることに成功した。このように、DNA結合性因子であって、ヌクレオソーム構造形成活性を有する因子の発見は世界的に初めてのことである。この発見は、ヌクレオソーム構造形成の制御も細胞の癌化・分化制御に重要であり、今までにない抗癌剤開発の対象となる反応となりうることを示唆し、抗癌剤開発に新しい道を示すものである。