炎症性細胞死の現場を捉える~単一細胞イメージングが明らかにした炎症応答のデジタル制御~研究成果

炎症性細胞死の現場を捉える |
平成26年8月8日
東京大学大学院薬学系研究科
1.発表者:
劉 霆 (東京大学大学院薬学系研究科 薬科学専攻 博士課程1年)
山口良文(東京大学大学院薬学系研究科 薬科学専攻 助教)
三浦正幸(東京大学大学院薬学系研究科 薬科学専攻 教授)
2.発表のポイント:
◆細胞の炎症応答に関与する「カスパーゼ-1」の活性化を検出するプローブを開発し、マクロファージにおいてカスパーゼ-1が活性化される様子を捉えた。
◆カスパーゼ-1の活性化動態およびその活性化によって引き起こされる炎症性サイトカインの分泌が、単一細胞レベルでは全か無かのデジタルな様式で制御されることを明らかにした。
◆本成果は、多くの自己炎症性疾患や慢性炎症が関わる病態における新たな治療戦略の基礎となることが期待される。
3.発表概要:
生物が細菌による感染あるいは損傷による組織の傷害を受けると、炎症応答をはじめとする免疫応答が起こります。その一つとして、インフラマソーム(注1)によってカスパーゼ-1(注1、2)が活性化され、最終的に炎症性サイトカインの分泌や炎症性細胞死(パイロトーシス、注3)が生じる経路が注目されています。インフラマソームによる炎症性サイトカイン分泌制御の破綻は、自己炎症性疾患やがん、糖尿病といった慢性炎症が関与する疾患の病態にかかわっていることが知られています。しかしながら、インフラマソーム-カスパーゼ-1経路の活性化が、単一細胞内でどのように生じるかについてはよく分かっていませんでした。
東京大学大学院薬学系研究科の劉 霆(りゅう てぃん)大学院生、山口良文助教、三浦正幸教授らは、カスパーゼ-1の活性化を可視化する蛍光たんぱく質プローブを用いた単一マクロファージの解析により、カスパーゼ-1が活性化された細胞では細胞死が起き、活性化されていない細胞では細胞死が起きないという観察結果を得ました。また、カスパーゼ-1が活性化されてから細胞死に至るまでの活性化の様子は刺激の種類や強度に依らずほぼ一定でした。これは、カスパーゼ-1の活性化によって引き起こされる炎症性サイトカインの分泌やそれに続く細胞死は、ひとつの細胞内では刺激の強さに応じて連続的(アナログ)に制御されているのではなく、全か無かのデジタルな様式で制御されることを示唆しています。さらに、単一細胞からのサイトカイン分泌を可視化した解析では、炎症性サイトカイン(IL-1β)の急激な放出がカスパーゼ-1活性化に続き非常に短い時間内に生じ、かつカスパーゼ-1を活性化した細胞のみから生じることが明らかとなりました。
今回明らかにしたインフラマソームを介したカスパーゼ-1活性化のデジタルな制御が、急性炎症のみならず、自己炎症性疾患、自己免疫性疾患やがん、糖尿病等の慢性炎症が関与する疾患の病態にも寄与している可能性があります。また、今回開発したプローブを用いてさまざまな急性および慢性炎症モデルマウスでインフラマソーム-カスパーゼ-1経路を可視化することで、生体内で炎症応答が単一細胞レベルでどのように制御されるかを解明することも可能であり、新たな病態発症機構の解明や治療法開発への発展が期待されます。
4.発表内容:
①研究背景
生物が細菌やウイルスによる感染を受けた時あるいは損傷によって組織に傷害が生じた時、炎症応答を初めとする免疫応答が惹起されます。近年、炎症応答を制御する重要な因子として免疫担当細胞からの炎症性サイトカイン分泌や炎症性細胞死を誘導するインフラマソーム-カスパーゼ-1経路が注目されています。インフラマソームによる炎症性サイトカイン分泌制御の破綻は、自己炎症性疾患、自己免疫性疾患やがん、糖尿病といった慢性炎症が関与する疾患の病態にかかわっていることが知られています。インフラマソームには複数の種類があり、多種多様な刺激に応答して活性化します。面白いことに、これら複数のインフラマソームは活性化されると共通してカスパーゼ-1の活性化を引き起こします。しかしながら、インフラマソーム-カスパーゼ-1経路の活性化が単一細胞内でどのように生じ制御されているのかについて、その詳細はほとんど分かっていませんでした。これは、単一の細胞を捉えることのできる高い解像度でカスパーゼ-1の活性化をリアルタイムに評価する手法が存在しなかったためです。こうした、単一細胞レベルでのカスパーゼ-1活性化動態を明らかにすることは、組織内の局所で生じる炎症応答がどのような影響を周辺細胞に与えるのか理解する上でも、非常に重要です。
酵素の活性やシグナル伝達を単一細胞内で捉えることのできる高い解像度をもつ蛍光プローブとして、蛍光たんぱく質間で生じるFRET(注4)を利用したものがあります。カスパーゼ-1の活性化をFRETプローブによって可視化することができれば、単一細胞レベルでインフラマソーム-カスパーゼ-1経路がどのような動態で活性化され、それがどのようにして細胞ひいては細胞集団の応答を引き起こすかを明らかにできると期待されていました。
②研究内容
今回、東京大学大学院薬学系研究科の劉霆大学院生、山口良文助教、三浦正幸教授らは、カスパーゼ-1の活性化を、FRETを利用して高解像度でリアルタイムに検出する蛍光タンパク質プローブ(SCAT1)を開発しました。このSCAT1を発現するマウスを作製しそのマウスから採取した腹腔マクロファージを用いることで、単一マクロファージにおいてインフラマソーム刺激によって活性化されるカスパーゼ-1の可視化に成功しました。さまざまな刺激を与えたのちにカスパーゼ-1の活性化が観察されたマクロファージではただちに細胞死がおこり、一方、活性化が認められなかったマクロファージでは細胞死を引き起こさないという明確な違いが観察されました。次に、与える刺激の強さや種類によって、カスパーゼ-1の活性化動態がどのように変化するかを調べました。インフラマソームには複数の種類があることが知られており、与えられた刺激の種類によって活性化されるインフラマソームの種類も異なりますが、そのアウトプットはいずれも共通でカスパーゼ-1の活性化です。単一細胞レベルでの定量解析の結果、活性化されたインフラマソームの種類あるいは与えた刺激の強度に依らず、カスパーゼ-1の活性化動態はほぼ一定でした。これらの結果は、カスパーゼ-1の活性化には細胞ごとに活性化に必要な刺激の値(閾値)が存在し、この閾値を超えてはじめてカスパーゼ-1が活性化されることを示唆しています(図右上)。最後に、「全か無か(デジタル性)のカスパーゼ-1活性化」と、インフラマソーム-カスパーゼ-1経路の最終段階である炎症性サイトカインIL-1βの分泌とが、どのように関連するかをカスパーゼ-1活性化とIL-1β分泌を同時に可視化できる手法により調べました。その結果、カスパーゼ-1活性化が見られた細胞でのみ、非常に短い時間内に急激なIL-1β放出(IL-1βバースト)が観察されました。以上の結果から、単一細胞内ではカスパーゼ-1はインフラマソーム刺激に対し全か無かのデジタルな様式で活性化し、この活性化がデジタルな炎症性サイトカインIL-1βの分泌をもたらすことが示唆されました(図)。
③今後の展望
炎症性サイトカインIL-1βは生体防御応答の主要な要素である一方、その分泌の制御破綻は多くの慢性炎症疾患につながる危険性も持ち合わせています。本研究で明らかになった、インフラマソーム-カスパーゼ-1経路からの刺激によって単一マクロファージからIL-1βが急激に放出されるIL-1βバースト現象は、局所的に生じる炎症性細胞死が周辺細胞の振る舞いに大きく影響を与える可能性を示唆しています。さらに、IL-1βバーストは急性のみならず慢性炎症においても重要である可能性があり、その制御を担う分子機構を解明することで新たな病態解明や治療法の開発に結びつくことを示唆しています。また、近年の単一細胞を用いた網羅的遺伝子発現解析から、同じ細胞集団であっても刺激に対する応答性は多様であることが明らかになってきました。本研究で開発したプローブを用いて、刺激に対して反応する細胞と反応しない細胞との間で、遺伝子発現や遺伝子産物の違いを網羅的に解析することにより、刺激に対する応答を可能にする遺伝子群を同定でき、全く新しい創薬標的の発見につながると期待されます。
なお、SCAT1を発現するマウスの作製は、理化学研究所統合生命医科学研究センター、星野克明客員主管研究員(現・香川大学教授)、改正恒康客員主管研究員(現・和歌山県立医科大学教授)らとの共同研究により行われました。また、炎症性サイトカインIL-1βの分泌を可視化する手法は、同センターの白崎善隆研究員、小原收グループディレクターらにより開発され、共同研究の一環として用いられました。
本研究は、文部科学省科学研究費補助金新学術領域研究「細胞死を起点とする生体制御ネットワークの解明」、文部科学省科学研究費補助金基盤研究(S)「発生頑強性を規定する細胞死シグナルの解明」、文部科学省科学研究費補助金新学術領域研究「内因性リガンドによって誘導される「自然炎症」の分子基盤とその破綻」の一環として行われました。
5.発表雑誌:
雑誌名:「Cell Reports」
出版・発行: 2014年8月7日(米国東部時間正午)
論文タイトル:Single-cell imaging of caspase-1 dynamics reveals an all-or-none inflammasome signaling response
著者: Ting Liu, Yoshifumi Yamaguchi*, Yoshitaka Shirasaki, Koichi Shikada, Mai Yamagishi, Katsuaki Hoshino, Tsuneyasu Kaisho, Kiwamu Takemoto, Toshihiko Suzuki, Erina Kuranaga, Osamu Ohara, and Masayuki Miura* (*:責任著者)
6.問い合わせ先:
東京大学大学院薬学系研究科 薬科学専攻 遺伝学教室
山口 良文(やまぐちよしふみ)助教、三浦 正幸(みうら まさゆき)教授
7.用語解説:
1)インフラマソーム:
細菌感染やストレスに応答する細胞内たんぱく複合体。刺激に応じて多くの種類が存在し、カスパーゼ-1の活性化を介してIL-1β等の炎症性サイトカインの分泌を制御する。クリオピリン関連周期性発熱症候群(CAPS)などの自己炎症性疾患との関与も知られている。
2)カスパーゼ-1:
たんぱく質分解酵素の一種。インフラマソーム内で活性化され、IL-1β等の炎症性サイトカインを切断することでその成熟・分泌を促進する。また、マクロファージなどの免疫担当細胞においては細胞死も誘導する。
3)炎症性細胞死:
マクロファージ等の免疫担当細胞でカスパーゼ-1が活性化されると、最終的に炎症性サイトカインが分泌され起きるプログラムされた細胞死の一種。炎症性サイトカインの分泌を伴う細胞死で、細菌が増殖する場を無くすといった生理的意義が知られている。パイロトーシスとも呼ばれる。
4)FRET(蛍光共鳴エネルギー移動):
近接した2つの発色団の励起エネルギーが電子の共鳴により直接移動する現象。発色団が蛍光分子の場合、一方の分子(供与体)で吸収された光エネルギーが他方の分子(受容体)に移動し、受容体から蛍光が発せられる。この現象を応用することで、さまざまな酵素の活性を可視化するプローブが作られている。
8.添付資料:
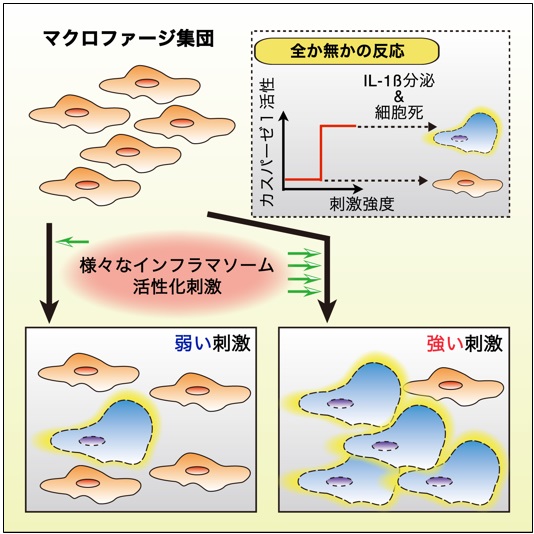
図 単一細胞におけるインフラマソーム-カスパーゼ-1経路のデジタル制御
右上:単一細胞レベルにおいて、カスパーゼ-1活性化には刺激の閾値が存在し、この閾値を超える細胞(青)でのみ炎症性サイトカインIL-1βの分泌および細胞死が起こり、超えない細胞(オレンジ)ではサイトカイン分泌も細胞死も起きない。
それ以外:細胞集団においては、刺激の強さに応じて反応する細胞の数のみが変化し、細胞単位での応答に大きな差はない。