アルドステロン拮抗薬が慢性腎臓病患者の蛋白尿を抑制することを証明 ―塩分を過剰摂取する日本人の慢性腎臓病に適した治療―研究成果

アルドステロン拮抗薬が慢性腎臓病患者の蛋白尿を抑制することを証明 |
平成26年10月28日
東京大学先端科学技術研究センター
1.発表者:
東京大学名誉教授 藤田 敏郎
(東京大学先端科学技術研究センター 臨床エピジェネティクス講座)
2.発表のポイント:
◆アルドステロン拮抗薬が慢性腎臓病患者のアルブミン尿を抑制することを二重盲検比較試験によって証明しました。
◆塩分摂取量の多い慢性腎臓病患者は、従来の治療薬に加えてアルドステロン拮抗薬の併用が効果的であることを明らかにしました。
◆難渋する慢性腎臓病の治療に有効な治療法となると期待されます。
3.発表概要:
慢性腎臓病(CKD)患者は放置すると将来腎不全となり人工透析を余儀なくされることから、CKDの対策と治療は喫緊の課題です。このたび、東京大学名誉教授 藤田敏郎(東京大学先端科学技術研究センター 臨床エピジェネティクス講座)を主任研究者とするEVALUATE研究グループ(用語解説1)は、血液中にあるナトリウムとカリウムの濃度を調節するアルドステロン(用語解説2)の働きを妨げるアルドステロン拮抗薬がCKD患者のアルブミン尿(用語解説3)を抑制することを二重盲検比較試験(用語解説4)によって証明しました。
藤田名誉教授らは先に、塩分摂取がアルドステロン受容体を活性化することにより腎障害を引き起こされることを動物実験によって明らかにしていました(参考文献1)。 今回、塩分摂取量の多い日本人のCKD患者にアルドステロン拮抗薬を投与したところ、腎臓障害の指標となるアルブミン尿が抑制されることが臨床研究の結果わかりました。この結果は、塩分摂取量の多いCKD患者では従来の治療薬だけではアルブミン尿の抑制は不十分であり、アルドステロン拮抗薬を併用することによってアルドステロン受容体の活性を抑制することが効果的であることを明らかにしたものです。これは、難渋するCKD治療の新たな展開を促すことになります。
本研究成果は、英国の科学雑誌「The Lancet Diabetes & Endocrinology」に掲載されるに先立ち、英国時間10月28日午前1時(日本時間10月28日午前10時)に、オンライン版に掲載されます。
4.発表内容:
慢性腎臓病患者(CKD)に対しては、腎障害の進行を抑制する目的で高血圧や糖尿病の治療薬であるレニン・アンジオテンシン(RA)系抑制薬が従来から投与されてきましたが、その効果は十分とは言えません。すなわち、高血圧や糖尿病の治療薬が繁用されているにもかかわらず、日本の慢性透析患者の数は増加の一歩を辿り、昨年(平成25年)末時点で患者数は30万を超えています。疫学調査から、塩分の過剰摂取がCKDの進行を早めることが知られていましたが、その機序の詳細については明らかでありませんでした。
2008年、藤田名誉教授らは塩分摂取がアルドステロン受容体の活性化を介して腎臓病の進行を促すことを世界に先駆けて明らかにしました(Nat Med 2008, JCI 2011、参考文献1,2)。日本は塩分摂取量が多いことから、CKD患者ではアルドステロン拮抗薬が有効であることが想定され、2009年から2012年にかけて、藤田名誉教授を主任研究者とするEVALUATE研究グループは、RA系抑制薬を投与中の高血圧を伴う非糖尿病性CKD患者(用語解説5)にアルドステロン拮抗薬を投与する臨床試験を行いました。この臨床試験は、日本では実施困難とされてきた医師主導の二重盲検比較試験です。その結果、アルドステロン拮抗薬を投与した実薬群では、偽薬を投与したプラセボ群に比べて尿中の蛋白質であるアルブミンの排泄が有意に減少しました(図1)。
更に、一日の塩分摂取量(尿中のナトリウム排泄量で換算)の多い患者ではアルドステロン拮抗薬の効果が有意に認められましたが、塩分摂取量の少ない患者ではその効果が認められませんでした(図2)。このことから、塩分摂取量が多いCKD患者ではRA系抑制薬のみでは不十分でアルドステロン拮抗薬の併用が必要であると示唆されました。一方、塩分摂取の少ないCKD患者ではRA系抑制薬の効果が良く発揮されることが分かりました。
現在、RA系抑制薬は高血圧を伴うCKD患者の第一選択薬として用いられていますが、塩分の過剰摂取により、その効果が半減することが知られています。本研究結果はこの“塩分摂取によるRA系抑制薬の不応性”の機序としてアルドステロン受容体の活性化が関与していることを示唆しており、これまでの藤田名誉教授らの基礎研究に基づく仮説を支持する結果です。
これまでに報告された世界の129の観察研究の結果から得られた一日の塩分摂取量の平均値の9.4グラムと比較して(参考文献3)、健康な日本人の一日の塩分摂取量は男性で12グラム、女性は10グラムと多く、日本の健康人推奨塩分量のそれぞれ8グラム、7グラムに比べて高い値です(参考文献4)。今回の研究でも患者の平均摂取量は12.8グラムでCKDや高血圧患者推奨塩分量の6グラムを遥かに超えて摂取していることが分かりました。その結果、日本における減塩運動の重要性が強調されるとともに、アルドステロン拮抗薬を用いたCKD治療戦略の新たな展開が期待されます。
但し、腎機能障害が中等度以上のCKD患者ではアルドステロン拮抗薬の副作用として、血液中のカリウムの濃度が高くなってしまう高カリウム血症を来たす危険性があるため、繰り返して血清カリウム濃度を測定する必要があります。本研究においては正常~軽度の腎機能低下(eGFR≧50)(用語解説6)の非糖尿病性CKD患者を対象として少量のアルドステロン拮抗薬を用いたため、重篤な高カリウム血症の発現は認められませんでした。一方、本薬はアルブミン尿を伴う糖尿病患者では高カリウム血症の副作用のため禁忌となっています。しかし、増加する糖尿病が透析導入の原因疾患の一位の座を占めており、かつ糖尿病性腎症に対して有効な治療法がない現状において、将来、糖尿病性腎症を対象として少量の本薬を用いたアルブミン排泄を抑制する効果、腎機能低下を抑制する効果及び副作用についての検討を目的とする二重盲検試験の実施が望まれます。
5.発表雑誌:
雑誌名:「The Lancet Diabetes & Endocrinology」(オンライン版:10月28日)
論文タイトル:
Anti-albuminuric Effect of an Aldosterone Blocker in Non-diabetic Hypertensive Patients with Albuminuria: A Double-blind, Randomized, Placebo-controlled Trial
著者: Toshiro Fujita, et al.
DOI番号:10.1016/S2213-8587(14)70194-9
6.問い合わせ先:
東京大学先端科学技術研究センター 臨床エピジェネティクス講座
東京大学名誉教授 藤田 敏郎
7.用語解説:
1. EVALUATE研究グループ:
EVALUATE試験を行った研究グループ。EVALUATE試験は、藤田敏郎名誉教授を主任研究者として全国59施設が参加した臨床試験(http://evaluate.umin.jp/top.html)で、そのコンセプト、方法論いずれにおいても、世界をリードする日本発の臨床試験です。550名のCKD患者スクリーニングから314名について統計解析が行われました。
(UMIN登録UMIN000001803)
2. アルドステロン
副腎皮質から分泌されるホルモンの一つであり、血液中におけるナトリウムとカリウムのバランスを調節する働きがあります。最も強力な鉱質コルチコイドであり、鉱質コルチコイド受容体(アルドステロンの受容体:MR)を刺激して、腎臓でナトリウムの再吸収(腎臓内で一度排泄された塩分が腎尿細管細胞内で取り込まれること)とカリウムの分泌を行います。副腎皮質腫瘍による原発性アルドステロン症では、アルドステロンの過剰分泌によって高血圧と血液中のカリウムの濃度が減ってしまう低カリウム血症を生じることが知られています。また、鉱質コルルチコイド受容体が活性化すると高血圧だけでなく、腎障害を生じることが知られていましたが、その機序の詳細は明らかでありませんでした。2008年、藤田名誉教授らはアルドステロンに依存しない鉱質コルチコイド受容体の活性化機構(Rac1-MR経路)を発見し(参考文献1)、塩分過剰による腎臓障害がRac1-MR活性化によることを世界に先駆けて明らかにしました(図3)。
3. アルブミン尿
尿に出てくる蛋白質の大部分はアルブミンで、アルブミン尿の測定は蛋白尿の測定より鋭敏に腎臓障害を反映します。慢性腎臓病患者(CKD)ではアルブミン尿の程度が腎症の予後(進行度)判定の指標となることが知られています。特に、糖尿病患者では尿中の微量アルブミンを測定すれば、早期に腎症を発見できます。一日の尿中アルブミン排泄量が30~300mgの場合を微量アルブミン尿、300mg以上の場合を顕性アルブミン尿と診断します。定期的に測定することで、腎症の進行の程度や現在服用中の薬の効果を判定できます。
4. 二重盲検比較試験
一般に、試験薬を投与された患者は薬を飲んだことを意識するため、そのことによる効果が出ます。これをプラセボ効果(偽薬であってもそれを薬として期待する)と呼びます。そこで、試験薬(実薬)と偽薬を患者から見て分からないようにして行う試験方法により真の薬効を判定します。しかしこの方法では観察者(医師)には区別がつくので、観察者が無意識であっても薬効を実際より高くまたは低く評価する可能性(観察者バイアス)や、患者に薬効があるかどうかのヒントを無意識的に与えてしまう可能性が排除できません。そこで、これをも防ぐために、観察者からもその性質を不明にする方法が二重盲検法です。本法を用いた臨床試験では、質は高くなりますが、患者の協力が必要であり、また試験にかかる費用が高いことから、これまでに日本で行われた医師主導の二重盲検比較試験は少ないのが現状です。
政策研ニュースNo.35によれば、日本から2008~2011年に発表された基礎論文(国際研究雑誌)の数は世界の第4位ですが、臨床論文の数は年々減少しており、世界の第25位に低迷しています(図4)。その原因の一つに医師主導の二重盲検比較試験が少ないことがあげられます。
5. 非糖尿病性CKD
慢性腎臓病(CKD)の原因疾患として糖尿病性腎症と非糖尿病性腎疾患があげられます。非糖尿病性腎疾患には慢性糸球体腎炎などの慢性糸球体疾患と高血圧による腎硬化症があります。いずれも放置すると、腎機能低下が進行し、最終的には末期腎不全に至り、人工透析を余儀なくされます。現時点では、高血圧や糖尿病の薬はありますが、CKDの進行を抑制する良い治療法がなく、CKD治療薬の開発が喫緊の課題です。
6. 糸球体濾過量GFR
腎臓の基本的な機能(腎機能)の良し悪しは、糸球体濾過量 Glomerular Filtration Rate (GFR) を用いて評価します。GFRは単位時間当たりに腎臓のすべての糸球体により濾過される血漿量のことで、血清クレアチニン値と年齢から求めるeGFR(estimated GFR; 推定糸球体濾過量)で代用することが多く、単位はml/分/1.73m2で表されます。慢性腎臓病(CKD)の病期(ステージ)は、eGFRに基づき、ステージ1(eGFR: 90~)、ステージ2(60~89)、ステージ3(30~59)、ステージ4(15~29)、ステージ5(~15)の5段階に分類されます。ステージ5まで進行した場合には、腎機能が著しく低下していることを示します。
8.参考文献:
1. Shibata S, Nagase M, Yoshida S, et al. Modification of mineralocorticoid receptor function by Rac1 GTPase: implication in proteinuric kidney disease. Nat Med 2008; 14(12): 1370–6
2. Shibata S, Mu S, Kawarazaki H, et al. Rac1 GTPase in rodent kidneys is essential or salt-sensitive hypertension via a mineralocorticoid receptor-dependent pathway. J Clin Invest 2011; 121(8): 3233–43.
3. McCarron DA, Kazaks AG, Geerling JC, et al. Normal range of human dietary sodium intake: a perspective based on 24-hour urinary sodium excretion worldwide. Am J Hypertens 2013; 26(10): 1218–23.
4. Asakura K, Uechi K, Sasaki Y, et al. Estimation of sodium and potassium intakes assessed by two 24h urine collections in healthy Japanese adults: a nationwide study. British J Nutrition 2014; 112(7): 1195-205.
9.添付資料:
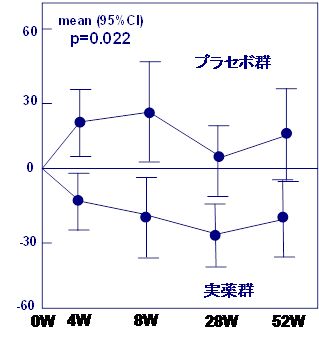
図1 アルブミン尿の減少率(実薬群とプラセボ群の比較)
縦軸がアルドステロン拮抗薬(実薬)または偽薬の投与による尿中のアルブミン排泄量の増加の度合いで、縦軸が投与期間(週)である。プラセボ群では投与前に比べてアルブミンの排泄量は減っていないが、実薬群では有意に減っており、アルドステロン拮抗薬の効果が認められる。

図2 アルブミン尿の減少率(低塩分摂取群と高塩分摂取群郡の比較)
縦軸はアルドステロン拮抗薬(実薬)または偽薬の投与による尿中のアルブミン排泄量の増加の度合いである。高塩分摂取群では、実薬群でアルブミン排泄量が減少しており、アルドステロン拮抗薬の効果が有意に認められるが、低塩分摂取群では、実薬群、プラセボ群ともに変化はほとんどなく、効果は認められない。
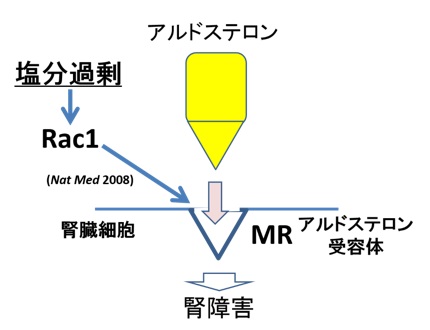
図3 塩分過剰がRac1によりMRが活性化する!
~アルドステロン非依存性のMR活性化機序~
アルドステロンは副腎皮質から分泌されるホルモンの一種で、血液中におけるナトリウムとカリウムのバランスを調節する働きがある。通常、アルドステロンが分泌されると、腎臓細胞にあるアルドステロン受容体(MR)が刺激され、腎臓でナトリウムの再吸収(腎臓内で一度排泄された塩分が腎尿細管細胞内に取り込まれること)とカリウムの分泌が促される。通常は血液のアルドステロンが高い時に、はじめてMRが刺激されるのですが、アルドステロンが低くてもMRが刺激されている病態(塩分過剰による高血圧や腎障害)があることが分かっていましたが、その機序は不明であった。2008年、藤田名誉教授らは塩分を過剰に摂取するとアルドステロンは低下するにもかかわらず、Rac1というタンパク質がMRを活性化し、ナトリウムの再吸収やカリウムの分泌を促進して、高血圧と腎障害を引き起こすことを世界に先駆けて明らかにした(Nat Med 2008)。
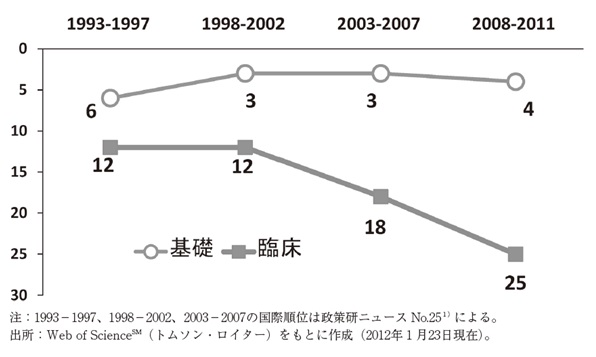
図4 基礎及び臨床論文数における日本の国際順位の推移
日本から2008~2011年に発表された基礎論文の数は世界の第4位だが、臨床論文の数は年々低下傾向にあると報告されている。(出典:日本製薬工業協会医薬産業政策研究所発行 政策研ニュース No.35P48、2012年3月)。原因の一つに医師主導の二重盲検比較試験が少ないことがあげられる。