ピロリ菌による胃がん発症リスクを決める機構 発がんタンパク質間の結合強度が決め手

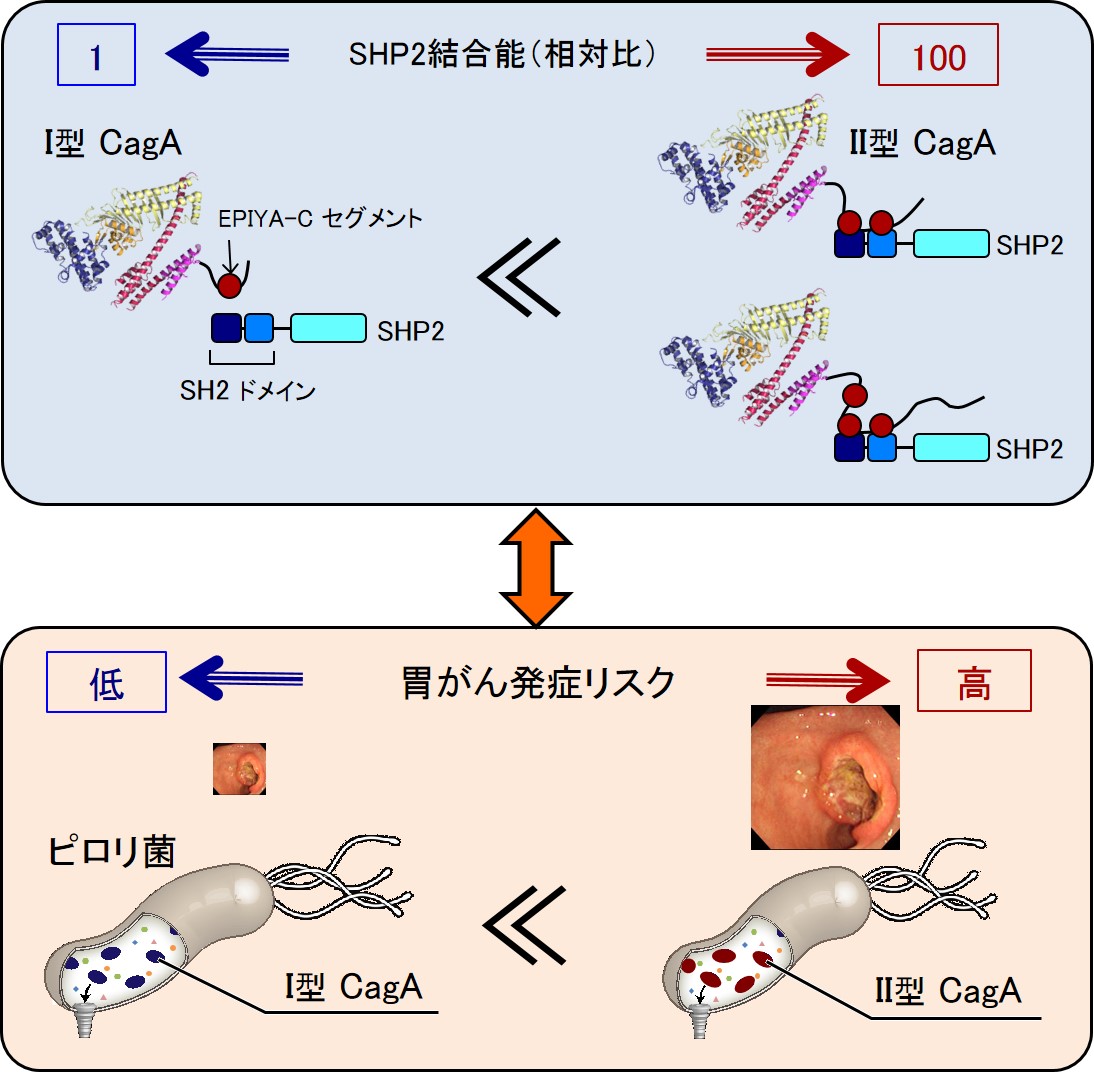
CagAのSHP2結合強度と胃がん発症リスクとの関係
EPIYA-Cセグメントを複数持つCagA (II型 CagA)はSHP2の二か所に結合できるため、安定した CagA-SHP2複合体を形成する。一方、単一のEPIYA-Cセグメントしか持たないCagA (I型 CagA)は一か所で結合するため、不安定なCagA-SHP2複合体を形成する。 このようなCagAと SHP2間結合の強弱が胃がん発症を規定する分子基盤となっている。
© 2015 東京大学 畠山昌則研究室
東京大学大学院医学系研究科 微生物学教室の畠山昌則教授らの研究グループは、ピロリ菌がんタンパク質CagAとヒトがんタンパク質SHP2間の結合の強弱が胃がんの発症リスクを決めていることを見出しました。本研究の成果は胃がん発症リスクの定量的な評価と効果的な胃がんの発症予防につながることが期待されます。
ピロリ菌が胃がんの発症に関与していることが知られていますが、ピロリ菌の中でもCagAと呼ばれるタンパク質を保有するピロリ菌が、胃がんと深く関わっていることがわかっています。CagAタンパク質は、ピロリ菌が保有する注射針様装置によって胃の上皮細胞内に注入されます。注入されたCagAは細胞膜内面に付着し、そこでがんタンパク質として働く脱リン酸化酵素であるSHP2と結合し、その酵素の活性を高めます。CagAタンパク質のSHP2結合部位は多様な形をとることが知られており、中でもEPIYA-Cセグメントと呼ばれる構造の数が、疫学的調査から、胃がんの発症に関与している可能性が示唆されていました。しかし、その分子的な基盤は明らかになっていませんでした。
今回、研究グループは、CagAタンパク質のEPIYA-Cセグメント数が1個から2個以上に増えることで、CagAタンパク質のSHP2に結合する強度が100倍以上増強することを明らかにしました。この結果からCagAを、単一のEPIYA-Cセグメント保有するI型(type I)と複数のEPIYA-Cセグメントを持つ2型 (type II)に分類しました。SHP2結合能の著しい差を反映し、II型CagAを発現させた胃の上皮細胞はI型CagAを発現する細胞に比較してはるかに強力な組織浸潤能を獲得しました。以上の結果から、同グループは、EPIYA-Cセグメントの重複によってCagAのSHP2へ結合する強度が飛躍的に増強することが 、ピロリ菌が胃がん発症を促す分子的な基盤であると結論付けました。
畠山教授は「CagAタンパク質は、SHP2との結合部位の形の違いから、欧米型(世界標準型)と東アジア型の二種に大別されます。今回の成果は、欧米型のCagAについて、調べたものです」と話します。「本成果から、胃がんハイリスク群の絞り込みを通した効果的な胃がんの発症予防が期待されます」と続けます。
論文情報
, "Dramatic increase in SHP2 binding activity of Helicobacter pylori Western CagA by EPIYA-C duplication: its implications in gastric carcinogenesis", Scientific Reports 5:15749: 2015/10/28 (Japan time), doi:10.1038/srep15749.
論文へのリンク(掲載誌)