新しいゲノム編集ツールCRISPR-Cas3の開発に成功 ヒトiPS細胞においてDMD遺伝子の修復に成功
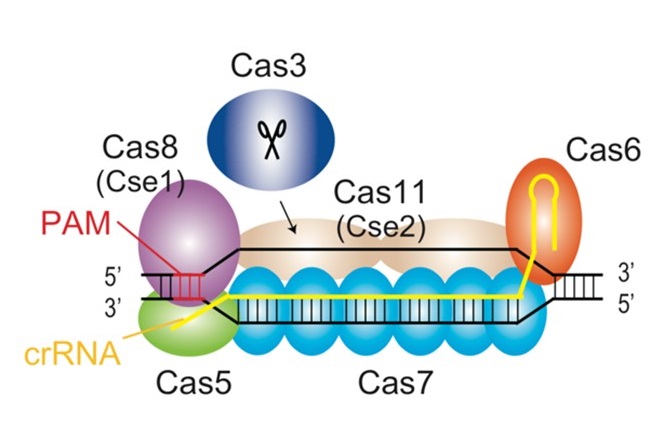
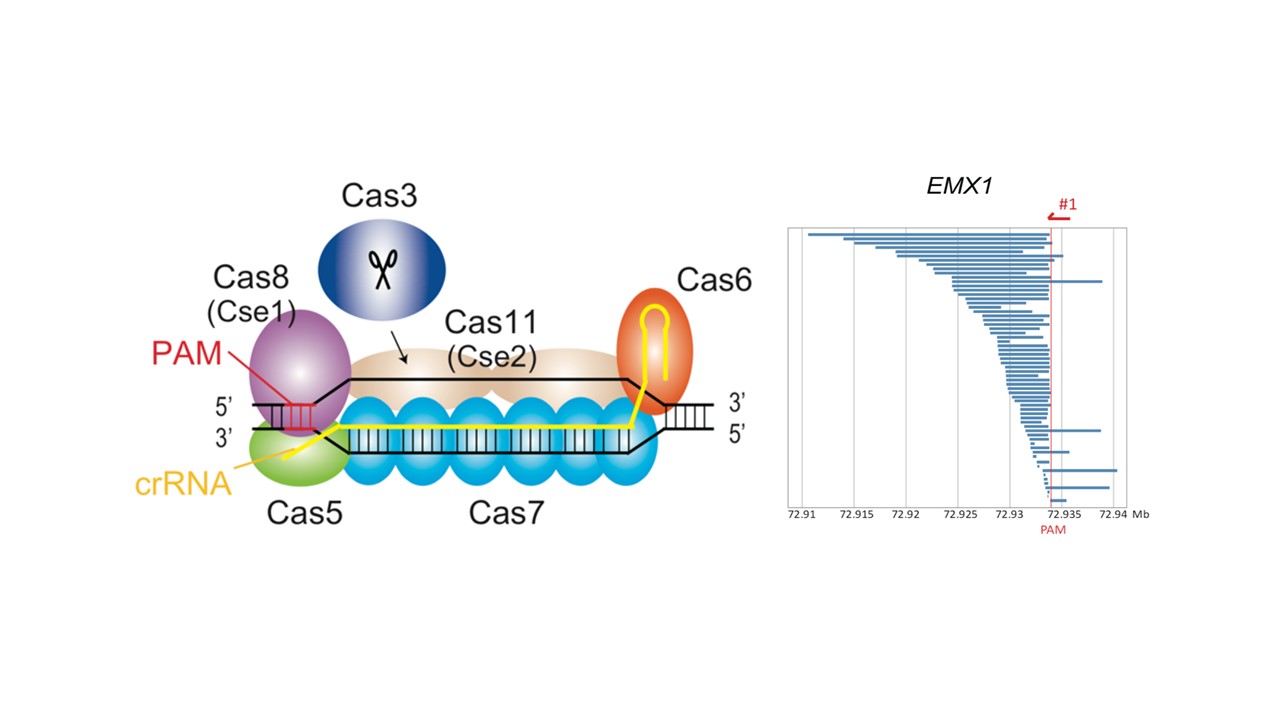
大腸菌由来CRISPR-Cas3の模式図(左)とキャプチャーシーケンス解析により同定されたEMX1領域に導入された欠失パターン(右)
© 2019 真下知士
東京大学医科学研究所/大阪大学医学部附属動物実験施設の真下知士教授、大阪大学微生物病研究所の竹田潤二招へい教授、京都大学iPS細胞研究所(CiRA)の堀田秋津講師らの研究チームは、新たに大腸菌由来Type I-E CRISPRシステム(CRISPR-Cas3)が、ヒト細胞でゲノム編集として利用できることを見い出しました。本研究成果は、英国科学誌「Nature Communications」に2019年12月6日付けで掲載されました。
CRISPR-Cas9を代表とするゲノム編集ツールは、さまざまなライフサイエンス分野に応用されています。一方でこれまでのゲノム編集技術は、狙っていない場所に変異が入るオフターゲット変異といった安全性への懸念や、知的財産の問題があり、新しいゲノム編集ツールの開発が求められていました。
CRISPR-Cas3は、狙ったゲノム配列の上流側を大きく削る性質を持ち、オフターゲットへの影響も極めて低いことも明らかにしました。さらに、デュシェンヌ型筋ジストロフィー(Duchenne muscular dystrophy: DMD)遺伝子に変異を持つヒトiPS細胞の遺伝子修復にも成功しました。
今回開発した日本発の新しいゲノム編集ツールCRISPR-Cas3システムは、従来よりも安全性が高く新たな創薬や遺伝子治療などへの利用、農水産物への利用などさまざまな分野で応用されることが期待されます。
「ゲノム編集は米国や中国を中心として、ものすごいスピードで技術開発や医療応用研究が進められています。今回、CRISPR-Cas9とは知財的にも独立した純国産のCRISPR-Cas3を開発することができ、ヒト細胞での効率的で安全性の高いノックアウトやノックインに成功したことで、日本でのこの分野の研究が一気に加速すると期待しています」と真下知士教授は話します。
論文情報
Hiroyuki Morisaka, Kazuto Yoshimi, Yuya Okuzaki, Peter Gee, Yayoi Kunihiro, Ekasit Sonpho, Huaigeng Xu, Noriko Sasakawa, Yuki Naito, Shinichiro Nakada, Takashi Yamamoto, Shigetoshi Sano, Akitsu Hotta, Junji Takeda and Tomoji Mashimo, "CRISPR-Cas3 induces broad and unidirectional genome editing in human cells," Nature Communications: 2019年12月6日, doi:10.1038/s41467-019-13226-x.
論文へのリンク (掲載誌 )
)