ピロリ菌が送り込む「尻尾のある刺客」 胃がん発症メカニズムがCagAタンパク質の構造から判明

胃がんは、全世界の部位別がん死亡の第二位です。世界中で毎年70万人もの命を奪うこの悪性腫瘍を引き起こす原因として、胃に棲み付いたピロリ菌が産出して胃細胞内に注射するCagAというタンパク質が、近年注目を集めています。
CagAは胃細胞内の様々な分子と相互作用して代謝を狂わせ、細胞をがん化させることが知られています。なぜ異物であるCagAにそのような機能があるのでしょうか。
一般に、タンパク質の機能はその構造と深く結びついていることが知られています。東京大学大学院医学系研究科の畠山昌則教授は産業技術総合研究所の千田俊哉主任研究員らと共に、X線結晶構造解析と核磁気共鳴法を用いて、CagAの3次元構造の決定に成功しました。
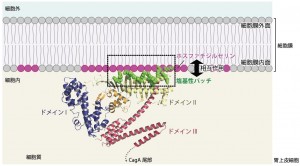
今回初めて明らかになったCagAの姿は、固いN字型構造の「CagA体部」と固有の構造を持たない「CagA尾部」から成るユニークなものでした。胃細胞内に侵入したCagAは、N字体部に存在する塩基性に富んだパッチ状の部分を使い、酸性を示す細胞膜内壁に静電気的な相互作用で付着し、尾部を垂らします。胃の細胞内で働いている複数の酵素はCagA尾部が持つアミノ酸の特徴的な繰り返し配列を目印にして、その部分にリン酸を付与します。これがカモフラージュの役割を果たし、細胞内のタンパク質は、CagAを異物と思わず相互作用してしまうのです。普段は決まった形を持たないCagA尾部が、この時は、特定のタンパク質と相互作用しやすい形に巧妙に変容して、効率よく細胞機能を暴走させていることがわかりました。
CagAが引き起こす細胞がん化のメカニズムを初めて解明した本成果により、今後、CagAに着目した創薬など、胃がん治療に新しいアプローチが加わることが期待されます。
(東京大学本部広報室 南崎梓,ユアン・マッカイ)
論文情報
Takeru Hayashi, Miki Senda, Hiroko Morohashi, Hideaki Higashi, Masafumi Horio, Yui Kashiba, Lisa Nagase, Daisuke Sasaya, Tomohiro Shimizu, Nagarajan Venugopalan, Hiroyuki Kumeta, Nobuo N. Noda, Fuyuhiko Inagaki, Toshiya Senda, and Masanori Hatakeyama
“Tertiary Structure-Function Analysis Reveals the Pathogenic Signaling Potentiation Mechanism of Helicobacter pylori Oncogenic Effector CagA”
Cell Host & Microbe 12, 20-33, July 19, 2012. doi:10.1016/j.chom.2012.05.010
Article link